Gehen Sie einen schnelleren, intelligenteren Weg zur KI-gestützten C/C++-Testautomatisierung. Erfahren Sie mehr >>
Navigieren in den FDA-Validierungsleitlinien für die Cybersicherheit medizinischer Geräte
Da die FDA weitere Anforderungen an ihre Cybersicherheitsvalidierung und -standards stellt, müssen Hersteller medizinischer Software statische Analysen einführen, um sicherzustellen, dass ihre Software diese neuen Sicherheitsstandards erfüllt. Lesen Sie weiter, um zu erfahren, wie Sie statische Analysen implementieren, um diese Sicherheitsanforderungen zu erfüllen.
Zum Abschnitt springen

Da die FDA weitere Anforderungen an ihre Cybersicherheitsvalidierung und -standards stellt, müssen Hersteller medizinischer Software statische Analysen einführen, um sicherzustellen, dass ihre Software diese neuen Sicherheitsstandards erfüllt. Lesen Sie weiter, um zu erfahren, wie Sie statische Analysen implementieren, um diese Sicherheitsanforderungen zu erfüllen.
Da die FDA ihre Richtlinien zur Softwarevalidierung um weitere Cybersicherheitsanforderungen erweitert, können Hersteller medizinischer Geräte auf die statische Analyse zurückgreifen, die effektivste Methode, um Sicherheitsbedenken auszuräumen und vorhersehbare Software bereitzustellen.
Hersteller medizinischer Geräte konzentrieren sich aus zwei Hauptgründen weiterhin auf die Verbesserung von Softwareentwicklungsprozessen.
Die neuen Leitlinien der FDA zur Cybersicherheit für medizinische Geräte wurden im September 2023 veröffentlicht und enthalten umfassende Empfehlungen für die Branche zum Design, zur Kennzeichnung und zur Dokumentation von Cybersicherheitsgeräten, die in Anträge vor der Markteinführung von Geräten mit Cybersicherheitsrisiko aufgenommen werden sollen.
Der Leitfaden soll Herstellern dabei helfen, Cybersicherheitsrisiken während des gesamten Lebenszyklus eines Medizinprodukts zu erkennen und zu mindern, vom Design und der Entwicklung bis hin zur Herstellung, Wartung und Überwachung nach dem Inverkehrbringen. Darüber hinaus werden Empfehlungen für die Kommunikation von Cybersicherheitsrisiken an Gesundheitsdienstleister und Patienten gegeben.
Die neuen Leitlinien bauen auf den früheren Leitliniendokumenten der FDA zur Cybersicherheit auf, enthalten aber auch eine Reihe neuer und aktualisierter Empfehlungen, wie zum Beispiel:
Früher konzentrierte sich die FDA auf Funktionssicherheit Aspekte der Systeme, aber jetzt Internet-Sicherheit ist ein Thema von gleicher Bedeutung. Auch wenn Safety und Security ähnlich sind – und man könnte leicht argumentieren, dass es bei beiden um die Entwicklung vorhersehbarer Software geht – betrachtet die FDA Cybersicherheit als etwas, das besondere Aufmerksamkeit und Maßnahmen erfordert.
Bei der Prozessvalidierung handelt es sich um die Sammlung und Auswertung von Daten, die den wissenschaftlichen Nachweis erbringen, dass ein Prozess in der Lage ist, dauerhaft ein Qualitätsprodukt zu liefern. Im Zusammenhang mit Medizinprodukten ist die Prozessvalidierung von entscheidender Bedeutung, um die Sicherheit und Wirksamkeit der Geräte über ihren gesamten Lebenszyklus hinweg zu gewährleisten.
Die Prozessvalidierung ist besonders wichtig für medizinische Geräte, die durch Software gesteuert werden, da Software komplex und schwer umfassend zu testen sein kann. Beispielsweise kann ein softwaregesteuertes medizinisches Gerät Millionen von Codezeilen umfassen, und es ist nicht möglich, jedes mögliche Szenario und jede mögliche Kombination von Ein- und Ausgängen zu testen, ohne beide zu nutzen statische Codeanalyse und dynamische Analyse.
Im Folgenden sind drei Hauptgründe aufgeführt, warum Prozessvalidierung wichtig ist.
Die in der FDA-Leitfaden zur Cybersicherheit medizinischer Geräte sollen den wachsenden Bedenken hinsichtlich der Sicherheit medizinischer Geräte in einem zunehmend vernetzten und digitalen Gesundheitsumfeld Rechnung tragen. Hier finden Sie eine Erläuterung der regulatorischen Anforderungen.
Die FDA verfügt nun über neue gesetzliche Befugnisse durch den Food and Drug Omnibus Reform Act (FDORA), der im Dezember 2022 in Kraft trat. Dieses Gesetz erlaubt es der FDA, bei der Einreichung von Medizinprodukten Informationen zur Cybersicherheit zu verlangen und verpflichtet Hersteller, konkrete Maßnahmen zu ergreifen, um die Cybersicherheit ihrer Geräte und zugehörigen Systeme hinreichend zu gewährleisten. Die Nichteinhaltung dieser Anforderungen gilt als verbotene Handlung und kann strafrechtlich verfolgt werden.
Der Begriff „Cybergerät“ wird im Gesetz neu definiert als ein Gerät, das vom Sponsor validierte, installierte oder autorisierte Software enthält, eine Internetverbindung herstellen kann und technologische Merkmale aufweist, die anfällig für Cybersicherheitsbedrohungen sein können. Diese Definition trägt dazu bei, zu klären, welche Geräte den neuen Cybersicherheitsanforderungen unterliegen.
Die neuen Leitlinien schreiben vor, dass Hersteller in ihren Anträgen vor der Markteinführung bei der FDA spezifische Informationen zur Cybersicherheit angeben müssen. Zu diesen Premarket-Einreichungen können Premarket Approval (PMA), 510(k)- oder De-novo-Einreichungen gehören. Die Cybersicherheitsinformationen sind erforderlich, um sicherzustellen, dass das Gerät die im Gesetz festgelegten Cybersicherheitsanforderungen erfüllt.
Gerätehersteller müssen einen Plan zur Überwachung, Identifizierung und Behebung von Cybersicherheitsschwachstellen und Exploits nach dem Inverkehrbringen vorlegen. Dieser Plan sollte den Ansatz des Herstellers zur kontinuierlichen Überwachung und Bewältigung von Cybersicherheitsrisiken darlegen, die nach der Markteinführung des Geräts auftreten können.
Hersteller müssen Prozesse und Verfahren entwickeln, aufrechterhalten und sicherstellen, dass das Gerät und die zugehörigen Systeme ausreichend „Cybersicherheit“ gewährleisten. Diese Anforderung unterstreicht die Notwendigkeit eines proaktiven Ansatzes, um Sicherheit in das Gerätedesign zu integrieren und über den gesamten Lebenszyklus des Geräts aufrechtzuerhalten.
Von den Herstellern wird erwartet, dass sie im Rahmen ihrer Einreichungen eine Software-Stückliste (SBOM) bereitstellen. In dieser Rechnung sollten die kommerziellen, Open-Source- und Standardsoftwarekomponenten aufgeführt sein, die im Gerät verwendet werden. Diese Informationen sind entscheidend für die Identifizierung und Behebung potenzieller Schwachstellen im Software-Stack.
Das Leitliniendokument ermächtigt die FDA außerdem, durch Vorschriften zusätzliche Anforderungen festzulegen, um nachzuweisen, dass das Gerät und die zugehörigen Systeme cybersicher sind. Hersteller müssen darauf vorbereitet sein, alle zusätzlichen Anforderungen der FDA zu erfüllen.
Ein wesentlicher Aspekt der regulatorischen Anforderungen ist die Aufnahme eines neuen gesetzlichen Verbotsgesetzes. Das bedeutet, dass die Nichteinhaltung der Cybersicherheitsanforderungen der FDA nicht nur ein Compliance-Problem, sondern auch einen Rechtsverstoß darstellt. Die Regierung ist befugt, Verstöße gegen diese Anforderungen strafrechtlich zu verfolgen oder Unterlassungsansprüche gegen nicht konforme Unternehmen geltend zu machen.
Hersteller von Medizinprodukten müssen viele Anforderungen erfüllen, um die Sicherheit, Wirksamkeit und Qualität ihrer Produkte zu gewährleisten. Wir werden uns mit den wichtigsten Aspekten der Einhaltung der FDA-Vorschriften für Medizinprodukte befassen, wobei wir einen größeren Schwerpunkt auf die Berücksichtigung von Sicherheitsbedenken bei Medizinprodukten und die Entwicklung von Kontroll- und Validierungsprotokollen für Hersteller legen.
Um die FDA-Vorschriften einzuhalten und der Patientensicherheit Priorität einzuräumen, müssen Hersteller medizinischer Geräte Sicherheitsbedenken wirksam angehen. Hier sind einige Tipps, um Sicherheitsbedenken bei medizinischen Geräten auszuräumen:
Richtige Designkontrollen und Validierungsprotokolle sind wichtige Bestandteile, um sicherzustellen, dass medizinische Geräte die regulatorischen Anforderungen der FDA erfüllen. Diese Kontrollen helfen Herstellern, sichere und wirksame Geräte zu entwickeln, die den Patienten die beabsichtigten Vorteile bieten.
Hier finden Sie wichtige Überlegungen zur Implementierung von Designkontrollen und Validierungsprotokollen.
Hersteller können verschiedene Tools und Methoden einsetzen, um die Einhaltung der FDA-Vorschriften für Medizinprodukte zu erreichen und aufrechtzuerhalten. Im Folgenden werden wesentliche Tools und Methoden besprochen, die bei der Verfolgung der FDA-Konformität hilfreich sein können.
Die statische Analyse spielt eine entscheidende Rolle dabei, Herstellern medizinischer Geräte dabei zu helfen, die strengen Anforderungen der FDA zu erfüllen.
Hier sind 5 Gründe, statische Analysen zur Erfüllung der FDA-Anforderungen einzusetzen.
Angesichts der Rolle des Risikomanagements bei der Erreichung der allgemeinen Ziele oder Anforderungen der FDA wollen wir uns damit befassen, wie Sie ein angemessenes Risikomanagement erreichen können.
Viele unserer Kunden von Medizinprodukten haben von Anfang an Erfolge bei der Einführung erzielt statische Analyse für C / C ++ indem Sie die folgenden Schritte ausführen:
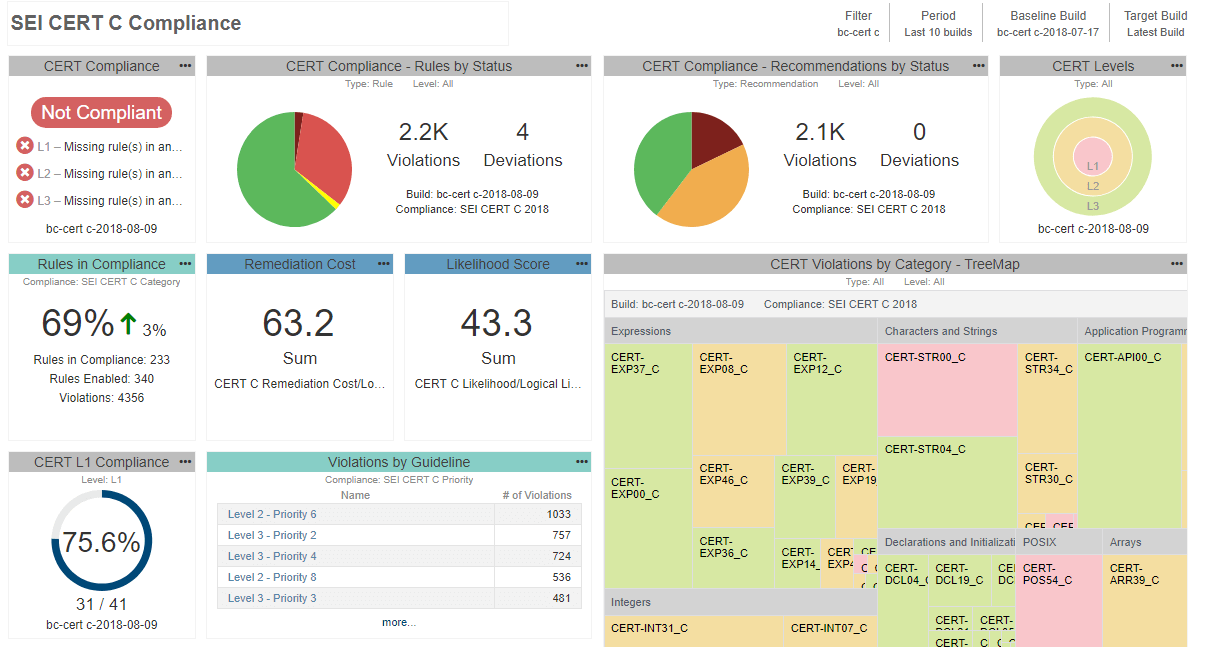
Da statische Analyseberichte Teil des Qualitätsmanagementsystems werden, können Sie nicht jedes beliebige Tool verwenden. Die FDA verlangt, dass alle bei der Entwicklung und Verifizierung der Software verwendeten Tools für den vorgesehenen Verwendungszweck validiert werden. Es gibt verschiedene Möglichkeiten, die Eignung des Tools für den Einsatz in sicherheitskritischen Entwicklungen nachzuweisen. Abhängig vom Risiko des Geräts kann es so einfach sein, ein Konformitätszertifikat wiederzuverwenden oder den längeren Prozess abzuschließen Werkzeugqualifikation.
Für den Endbenutzer ist es am bequemsten, die Gutschrift für die vom Werkzeughersteller geleistete Arbeit zu erhalten und die Zertifizierung, die von einer externen Zertifizierungsorganisation wie TÜV SÜD für das Testwerkzeug erteilt wurde, wiederzuverwenden. Parasoft C / C ++ test, zum Beispiel, ist mit abgedeckt eine TÜV SÜD-Zertifizierung die wiederverwendet werden können, um die Eignung für die Entwicklung von Software nach medizinischen Standards nachzuweisen, wie IEC 62304.
Für Hochrisikogeräte wie Klasse C müssen Sie das Tool möglicherweise intern in Ihrer Entwicklungsumgebung validieren. Ziel ist es, den Nachweis zu erbringen, dass das Tool gemäß seinen in der Entwicklungsumgebung des Projekts gesammelten betrieblichen Anforderungen funktioniert. Dies ist ein sehr langwieriger und zeitaufwändiger Prozess.
Am besten ist es, wenn Ihr Tool-Anbieter Sie bei diesem Vorhaben unterstützen und ein spezielles Tool-Qualifizierungskit bereitstellen kann, das gut gestaltete Testfälle und das Automatisierungs-Framework enthält, um diese in der Entwicklungsumgebung des Projekts auszuführen und automatisch die Dokumentation zu generieren, die als dienen kann der Beweis für die Werkzeugvalidierung. Auch hier bietet Parasofts Flaggschiffprodukt C/C++test eine automatisiertes Werkzeugqualifizierungskit.
Wir verfügen über eine Fülle von Fallstudien zu realen Anwendungen der statischen Analysetools von Parasoft. Aber schauen wir uns zwei unterschiedliche Erfolgsgeschichten an, die veranschaulichen, wie unsere Lösung für die statische Analyse eine wichtige Rolle dabei gespielt hat, Herstellern medizinischer Geräte dabei zu helfen, ihre einzigartigen Herausforderungen zu meistern und die FDA-Anforderungen zu erfüllen.
Die folgenden Fallstudien veranschaulichen, wie die Softwaretestlösungen von Parasoft maßgeblich dazu beigetragen haben, Hersteller medizinischer Geräte bei der Bewältigung ihrer einzigartigen Herausforderungen und beim Erreichen ihrer Ziele zu unterstützen. Inovytec und Smiths Medical verzeichneten durch ihre Zusammenarbeit mit Parasoft beide bemerkenswerte Verbesserungen bei der Codequalität, Compliance und Testeffizienz.
Inovytec, ein Unternehmen, das sich auf die Herstellung medizinischer Geräte spezialisiert hat, hat sich zum Ziel gesetzt, die FDA 510(k)-Zertifizierung für sein Beatmungsgerät Ventway Sparrow zu erhalten. Ihre Herausforderung bestand darin, sauberen Code zu liefern und gleichzeitig die FDA-Vorschriften einzuhalten. Die statische Codeanalyselösung C/C++ von Parasoft kam ihnen zu Hilfe.
Das Softwareentwicklungsteam von Inovytec hat den Parasoft C/C++-Test angepasst, um ihn an die strengen FDA-Anforderungen anzupassen. Jedes Mal, wenn sie sich auf die Veröffentlichung einer neuen Softwareversion vorbereiteten, stellten sie sicher, dass die statische Analyse von Parasoft so konfiguriert war, dass sie gemäß den Definitionen der FDA-Verordnung ausgeführt wurde. Das Ergebnis war nicht nur eine verbesserte Codequalität, sondern auch ein durchschlagender Erfolg bei der 100-prozentigen Erfüllung der FDA 510(k)-Zertifizierungsregeln und -richtlinien. Parasoft erwies sich bei Inovytec als bevorzugte Testlösung und die Zusammenarbeit mit ESL, einem Vertriebshändler für Parasoft-Produkte in Israel, bot bei Bedarf wichtige Unterstützung und Fachwissen.
Smiths Medical, ein renommierter Hersteller von medizinischen Spezialgeräten, sah sich bei seinem Bestreben, qualitativ hochwertige, sicherheitskritische Geräte zu entwickeln, mit einer Reihe von Herausforderungen konfrontiert Software für medizinische Geräte. Automatisierte Tests spielen eine entscheidende Rolle in der Teststrategie von Smiths Medical.
Frühere Bemühungen, Tools zu integrieren, waren nicht von vollem Erfolg. Das Entwicklungsteam suchte nach einer Lösung, die seinen gesamten Testprozess verbessern könnte, indem es eine neue Perspektive einnimmt, die sich auf Unit-Tests und testgetriebene Entwicklung (TDD) konzentriert, eine Methodik, die Design, Tests und Codeentwicklung integriert. Sie brauchten ein Tool, das in ihre Testpipeline passt und ihre gesamte Entwicklungskultur verbessert. Parasoft C/C++test erwies sich als die Antwort auf ihre Herausforderungen.
Das Softwareteam erzielte nicht nur eine erfolgreiche TDD-Einführung, sondern profitierte auch von einer verbesserten Teststabilität, einer verbesserten Codeabdeckung und einem optimierten Tool-Qualifizierungsprozess, was für sicherheitskritische Anwendungen von entscheidender Bedeutung war. Mit Parasoft war Smiths Medical in der Lage, seine Entwicklungsprozesse zu transformieren, Tests zu einem integralen Bestandteil seiner Software-Pipeline zu machen und letztendlich die Lieferung sicherer, qualitativ hochwertiger medizinischer Geräte sicherzustellen.
Der FDA-Validierungsprozess kann für Hersteller medizinischer Geräte komplex und herausfordernd sein. Es gibt jedoch eine Reihe von Maßnahmen, die Hersteller ergreifen können, um diese Herausforderungen zu meistern.
Die FDA stellt Herstellern medizinischer Geräte wichtige Validierungsrichtlinien zur Verfügung, um Produktqualität und Patientensicherheit sicherzustellen. Da sich Vorschriften und Richtlinien weiterentwickeln, ist es von entscheidender Bedeutung, über diese Änderungen auf dem Laufenden zu bleiben und die zukünftige Einhaltung zu planen. Medizingerätehersteller können dies auf zweierlei Weise erreichen: indem sie sich auf zukünftige FDA-Richtlinien vorbereiten und diese einhalten.
Die FDA aktualisiert und überarbeitet ständig ihre Leitliniendokumente für Hersteller von Medizinprodukten. Um sich auf zukünftige FDA-Richtlinien vorzubereiten, sollten Hersteller medizinischer Geräte:
Hersteller medizinischer Geräte müssen die kontinuierliche Einhaltung der FDA-Vorschriften sicherstellen. Um dies zu erreichen, sollten Hersteller:
Im Laufe der Zeit hat sich das Erreichen der FDA-Konformität als recht streng und zeitaufwändig erwiesen. Mit statischen und dynamischen Analysetools können diese Herausforderungen jedoch gemeistert werden. Statische Analysetools bieten erweiterte Funktionen zur statischen Codeanalyse, die dabei helfen, Probleme in Software und Code frühzeitig im Entwicklungsprozess zu erkennen und zu beheben.
Die Einführung einer statischen Analyse ist ein besonderer Aufwand, der Entwicklerzeit und -kosten erfordert. Aber es ist eine bewährte Methode, Ihr System gegen böswillige Angriffe abzusichern. Durch den Einsatz einer statischen Analyse mit gut durchdachten Sicherheitsrichtlinien können Sie Systeme aufbauen, die unvorhergesehenen zukünftigen Angriffen standhalten können.
„MISRA“, „MISRA C“ und das Dreieckslogo sind eingetragene Marken von The MISRA Consortium Limited. ©The MISRA Consortium Limited, 2021. Alle Rechte vorbehalten.